感度比較
B型肝炎ウイルス抗原, HBsAg ( hepatitis B virus antigen)
臨床的意義
B型肝炎ウイルス(HBV)は直径42nmの球形粒子で、外被(envelope)にHBs抗原(hepatitis B surface antigen)、内部(core)にHBc抗原(hepatitis B core antigen)と約3,200塩基対からなる環状二本鎖DNAを有する。さらに、HBVの増殖が盛んな時期には感染者の血液中に、可溶性蛋白であるHBe抗原(hepatitis Be antigen)が分泌される。現在、臨床的に測定されるHBVのウイルスマーカーには、HBs抗原・抗体、Hbe抗原・抗体、HBc抗体とIgM型HBc抗体がある。近年、PCR法による微量なウイルスの存在診断や、HBVのpre-C領域に変異をもつHBe抗原非産生ウイルスの発見などにより、ウイルスマーカーの解釈の仕方がやや複雑になってきたが、本質的には従来の考え方とほぼ同様である。B型肝炎感染には、一過性感染(急性肝炎、劇症肝炎)、無症候性キャリアから慢性肝炎、肝硬変、肝癌まで多様な臨床病態がみられるため、各種ウイルスマーカーの組み合わせによる正しい病態の把握が必要である。
① 現在のHBV感染の有無 : HBs抗原
a. 一過性感染 : IgM型HBc抗体価
b. HBVキャリア : HBc抗体価
② HBV感染の既往の有無 : HBc抗体、HBs抗体
③ HBV増殖状態 : HBe抗原、HBe抗体、HBV-DNA
一般臨床においては、まずHBs抗原を測定し、陽性であればB型肝炎と診断し得る。さらに、一過性感染の場合、IgM型HBc抗体が感染初期から陽性化し以後漸減するため、B型急性肝炎の診断に用いられる。B型慢性肝炎の急性増悪時にも、IgM型HBc抗体を検出し得るが、急性肝炎時より抗体価は低値であり鑑別はほぼ可能である。IgG型HBc抗体は感染成立後は年余にわたって血中に存在するため、抗体陽性の場合は既感染の場合と、持続感染(HBVキャリア)の双方の可能性があるが、HBc抗原は免疫系での抗体刺激・産生能がきわめて高いため、通常HBVキャリアではHBc抗体価は非常に高値で、200倍希釈での測定値が95%以上を示すことが多い。しかし、HBVキャリアであっても肝障害をまったく経験していないと考えられる例では、HBc抗体価(200倍希釈)の測定値が低値(70%以下)を示す場合もある。HBe抗原はHBV遺伝子のpre-C-C領域から作られる抗原蛋白で、HBV増殖時に産生される。一般にHBe抗原陽性の場合、肝内でのウイルス増殖が盛んで、血中のHBV量も多く感染力が高い。従来はHBe抗原の陰性化、さらにはHBe抗体の陽性化とともにB型慢性肝炎は鎮静化に向かうと考えられてきたが、pre-C領域やcore promotor領域に変異を有するHBe抗原非産生株(mutant HBV)の存在が明らかになり、HBe抗原消失の機序として、①HBe抗原産生ウイルスの量の減少、②HBe抗原産生ウイルスから非産生mutant HBVへのゲノムコンバージョン、の両者を考慮せねばならない。特にHBe抗原消失後も肝炎が持続する場合は、後者を考え、DNAプローブ法やTMA(transcription mediated amplification)法を用いたHBV-DNA定量や、mutant HBVを直接検出する方法の併用が必要である。HBs抗体はウイルスに対する中和抗体であり、HBs抗体が陽性である場合は肝炎が終息した既感染状態と考えられる。しかし、最近、B型慢性肝炎の鎮静化後にHBs抗原が陰性化し、症例によってはHBs抗体が陽性になった例でも、微量のHBV-DNAが肝内あるいは血中にも存在するという報告がなされており、このような場合にはHBc抗体価を含めた評価が不可欠となる。
測定方法: CLEIA法(RPHA法・EIA法は、ECLIA法に変更その後CLEIA法に変更, RIA法オーサブ(ダイナボット)RI法は平成13年1月4日から試薬発売中止に伴い中止)
測定試薬: スクリーニング法(旧RPHA): ルミパルスL2400(平成29年5月8日より)
ルミパルスプレスト(平成21年10月19日より平成29年5月2日まで)
CLEIA法(富士レビオ ルミパルスf)(平成16年10月4日より平成21年10月16日まで)
ECLIA法(ロシュ)(平成14年4月1日より平成16年10月1日まで)
エルジア・F-HBs抗原(国際試薬)(平成14年3月31日まで)
セロディア-HBs(富士レビオ)(平成13年9月30日まで)
精密測定法 : ルミパルスL2400(平成29年5月8日より)
ルミパルスプレスト(平成21年10月19日より平成29年5月2日まで)
CLEIA法(富士レビオ ルミパルスf)(平成16年10月4日より平成21年10月16日まで)
ECLIA法(ロシュ)(平成14年4月1日より平成16年10月1日まで)
エルジア・F-HBs抗原(国際試薬)(平成14年3月31日まで)
基準範囲: スクリーニング法 : (-)
精密測定法 :0.005 IU/mL未満(平成29年5月8日より測定機器および試薬変更)
1.0 COI 未満(平成29年5月2日まで)
(平成14年4月1日より平成16年10月1日まではECLIA法:基準範囲変更なし)
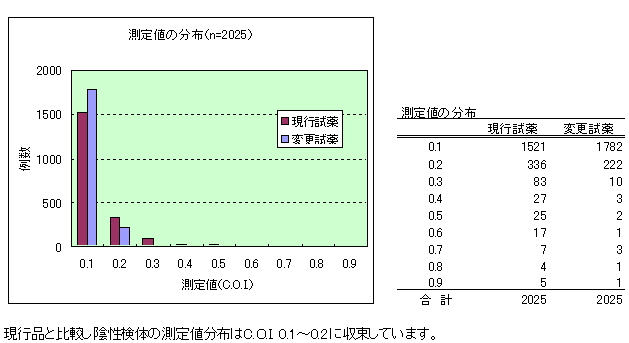
2006年8月7日(月)よりHBs抗原測定試薬について、特異性を改善した製品へ試薬を変更。変更品は現行品と同様にC.O.I. 1.0以上を陽性とする定性試薬です。C.O.I.は0.1~2000.0までが数値出力されますが、現行品と比較し高値検体で約30%程度C.O.I.が上昇します。
特異性比較

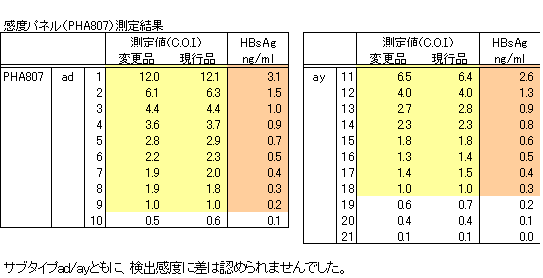
感度比較
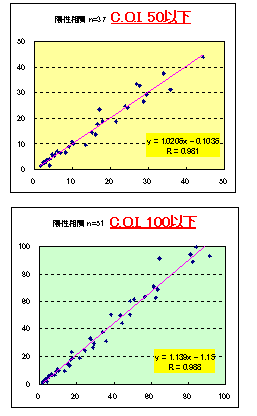
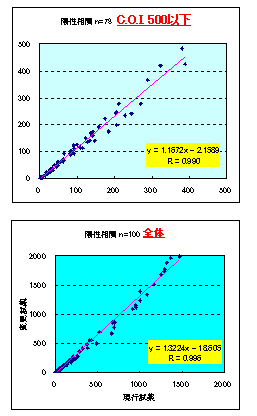
陽性検体相関
従来法との一致率
(平成29年5月8日)
| HBsAg(C.O.I) | ||||||||
| 陽性 | 陰性 | total | ||||||
| HBsAg-HQ (IU/mL) |
陽性 | 83 | 2 | 85 | ||||
| 陰性 | 0 | 26 | 26 | |||||
| total | 83 | 28 | 111 | |||||
| 一致率98.2%(109/111) | ||||||||
| *判定不一致の5例について確認 | ||||||||
| HBeAg (C.O.I.) |
HBeAb (%) |
HBcAb (C.O.I.) |
抑制試験 | |||||
| ID27 | 0.1 | 100 | 184.9 | 陽性 | ||||
| ID28 | 0.1 | 99.8 | 162.3 | 陽性 | ||||
(平成21年10月19日)
| HBsAg | 一致率 100% (117/117) | ルミパルスƒ | ||
| 精密検査 | 陽性 | 陰性 | ||
| ルミパルスプレスト | 陽性 | 58 | 0 | |
| 陰性 | 0 | 59 | ||
(平成16年10月4日)
| HBsAg | 一致率 99.6% (461/463) | エクルーシス | ||
| スクリーニング | 陽性 | 陰性 | ||
| ルミパルスƒ | 陽性 | 10 | 2 | |
| 陰性 | 0 | 451 | ||
| HBsAg | 一致率 97.0% (98/101) | エクルーシス | ||
| 精密検査 | 陽性 | 陰性 | ||
| ルミパルスƒ | 陽性 | 49 | 3 | |
| 陰性 | 0 | 49 | ||
採取容器:茶)生化学一般用分離剤入り試験管
関連項目
HBs抗体
HBe抗原
HBe抗体
HBc抗体