岡山大学大学院ヘルスシステム統合科学研究科/工学部化学生命系学科
生体分子工学研究室(大槻研)
![]()
研究内容
![]()
生体分子(タンパク質、ペプチド、RNAなど)をもとにした新規機能分子や分子ツールを創り、生命現象の解明や細胞機能の制御に役立てるとともに、医療応用も目指しています。 興味を持っている生命現象は、タンパク質生合成系、小分子RNAによる翻訳制御系、ストレス応答機構、細胞周期、細胞分化、初期発生、アポトーシス、エンドサイトーシスなどです。 医学部の先生との共同研究により、医薬の送達(ドラッグデリバリー)に関する研究も行っています。
広く生命科学研究に役立つ分子ツール(分子の道具)や基盤的な技術を開発することが中心的課題です。 生命の中心的役割を担うRNAやタンパク質に関する“基盤的な技術”をつくれば、あらゆる生命現象の解明に役立てることができるし、医学・薬学・農学的な実用化研究にも結び付けることができます。 工学系バイオ研究者は「何らかの産業に役立てばよい」という極めて緩い制約のもとで研究できるため、幅広い可能性につながる基盤的かつ独創的な技術を創ることがミッションだと考えています。 以下に最近の研究例を紹介します。
RNAおよびペプチド/タンパク質の細胞内送達
RNAおよびペプチドの細胞内送達法は、生命科学研究において広く利用可能であり、医薬としてのRNAやペプチドの運搬法としても期待できます。 当研究室では、細胞透過性ペプチド(CPP)を介した機能性ペプチド/タンパク質やRNA(shRNA、miRNA、non-coding RNAなど)の細胞内送達のための効率的な方法を検討しています。 さらに、光や超音波などの外部刺激に依存的な細胞内分子送達法についても研究しています。
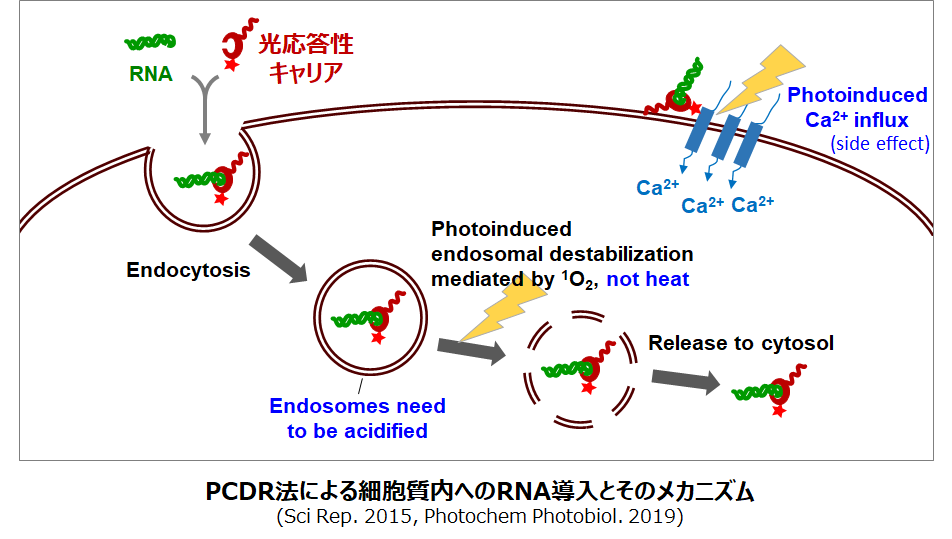
光化学的内在化 (photochemical internalization; PCI)
エンドサイトーシス経路で分子/薬剤を細胞内送達する際、エンドソーム内に捕捉されてしまうことが主な問題となります。 PCIは、この問題を回避する手段の1つであり、光増感剤を用いて光依存的に捕捉分子をエンドソームから細胞質内へと脱出させる方法です。当研究室では未だ不明点も多いPCIの分子メカニズムを研究するとともに、PCIに基づく生体分子/薬剤送達法(たとえばRNAを運ぶためのPCDR法)を開発しています。
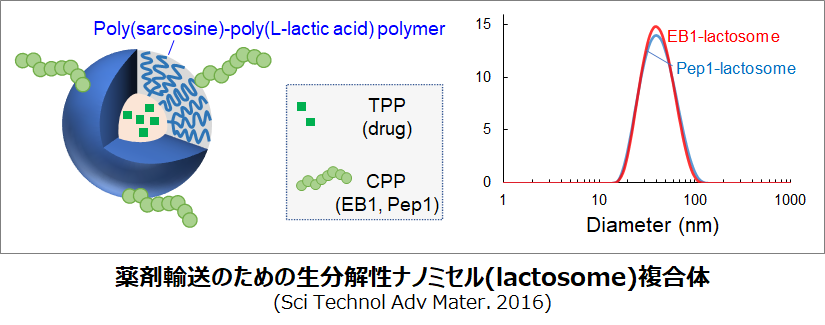
ドラッグデリバリーのためのナノ複合体
疾患部位に効率よく薬剤送達するためのナノ複合体を作っています。たとえば、ペプチド-RNAナノ複合体や高分子ナノミセルなどをベースとして、がんや動脈硬化の治療薬を運ぶためのキャリアを作っています。適度なナノサイズの粒子は、血流に乗ってEPRと呼ばれる効果により腫瘍組織内に蓄積する傾向があり、特にがん治療薬の送達に適しています。
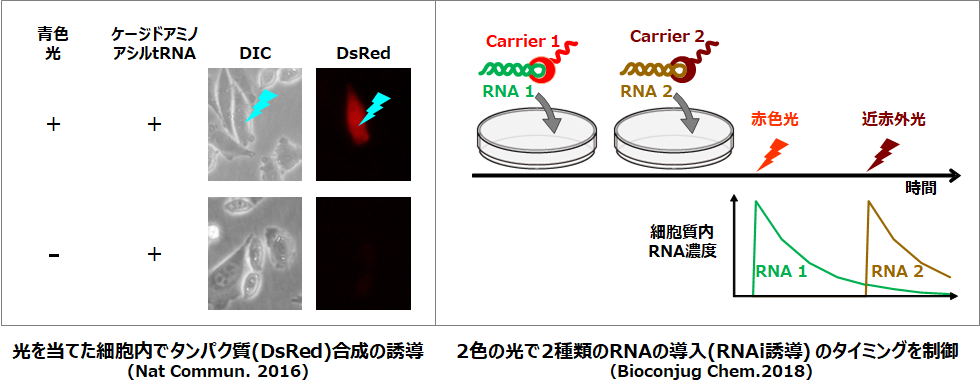
翻訳やRNAiの光制御
最近、タンパク質合成(翻訳)を光でONにする技術として、光で活性化するケージドアミノアシルtRNAを用いる方法を創りました。ケージドアミノアシルtRNAに光を当てると、翻訳に必要なアミノアシルtRNAが生じて翻訳が起こるという原理で、特定のタンパク質の合成を光で誘導することができます。また、当研究室では、光でRNAiを誘導する方法(CLIP-RNAi法)を開発しています。RNAiとは、siRNAやshRNAにより狙った遺伝子の発現を抑える方法であり、遺伝子機能や創薬の研究に広く利用されています。 このように、翻訳やRNAiを時空間的に光で制御することができれば、生体組織内における“局所”的なタンパク質/遺伝子の役割解明や生命システムの“時間”依存(細胞周期や発生など)に関する研究に応用できるようになると考えています。
非天然アミノ酸を導入するための翻訳系の拡張
タンパク質の中の狙った部位に非天然アミノ酸を導入する技術により、天然20種類のアミノ酸だけでは作れないような、新規でユニークな機能をもつタンパク質が作れます。当研究室では、tRNAを改良したり翻訳因子を改変したりすることで、非天然アミノ酸の導入効率改善や導入できる非天然アミノ酸の多様化に取り組んできました。 この方法を応用した、タンパク質の機能改変やタンパク質ベースの創薬スクリーニングなどが期待されます。
RNAの検出法
RNA検出法は、RNAの生物学的役割を調べる上で必要であり、医学的診断にも役立ちます。特に、細胞を壊さずに細胞内のRNAを検出する方法を検討しています。また、蛍光寿命によりRNA分解を検出するための方法を最近作りました。
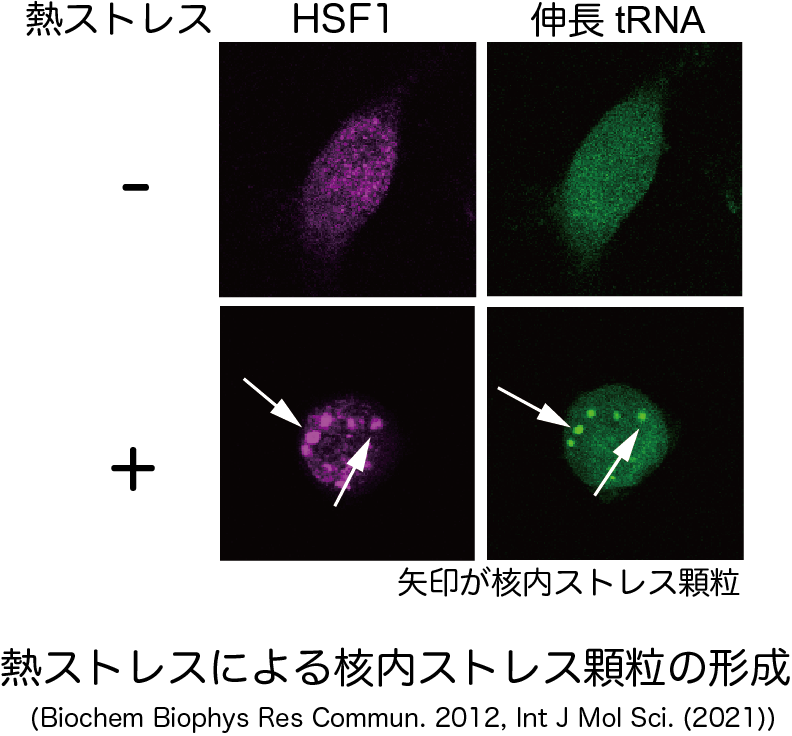
熱ストレス応答機構
細胞の熱ストレス応答の分子メカニズムについて研究しています。たとえば熱ストレスにより、特定のtRNA分解が亢進することでタンパク質合成が抑制されることを発見しました。現在、tRNA分解の亢進にどのような酵素が関与しているのか調べています。また、熱ストレスにより細胞内で相分離を起こすことで形成される核内ストレス顆粒の形成機構についても調べています。さらに、がん治療法の1つであるハイパーサーミアによる治療効果を高めるために、ストレス顆粒形成抑制剤の探索も行なっています。