ホーム > 修了生・同窓生の方 > 生物学科の学生活動報告(寄付金報告) > 奨学金受賞者(2026年度)
奨学金受賞者(2026年度)
2026年4月大学院博士後期課程に進学した優秀な学生に、この寄付金から奨学金が授与されました。受賞者の4人に研究内容をこのページで紹介してもらいました。時間生物学研究室:相川紗英「脳の時計が刻む“生き残るためのタイミング”」
【研究背景:なぜ生物は「時計」をもつのか?】私たち人間を含め、地球上のほとんどの生物は、約24時間周期で時を刻む「概日時計(体内時計)」を持っています。朝になると目が覚め、夜になると眠くなるのは、この時計が環境変化に合わせて私たちの体を整えているからです。
しかし、「時計が狂うと、自然界で生き残る力(適応度)が具体的にどう低下するのか?」という問いに対して、決定打となる研究は不足していました。その理由は、従来の実験では時計を壊すと体全体の様々な機能まで一緒に壊れてしまい、純粋に「時計のズレ」だけの影響に焦点を当てることが難しかったからです。
【研究内容:脳の時計だけを操作する新しい挑戦】
私は、モデル生物であるキイロショウジョウバエを用いて研究を行っています。キイロショウジョウバエは、体内時計の研究が最も進んでいる生物種で、2017年にノーベル賞を受賞しています。以下の2点が本研究の特徴です。
① 全身ではなく、脳の中にある「時計の司令塔」となる特定の神経細胞だけで、時計の進むスピードを速めたり遅めたりすることに成功しました。これにより、体の他の機能への影響を最小限に抑えつつ、純粋に「時間のズレ」の影響を調べることが可能になりました。
② 時計の速さが異なるハエたちを同じ場所で競わせ、どちらがより多くの子孫を残して生き残るかを、何世代にもわたって(人間で例えると数百年分に相当する期間)観察しました。キイロショウジョウバエでは世代交代が約12日で起こります。この短い世代サイクルによってこの研究が可能になります。
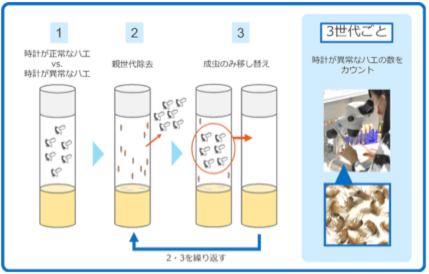
【今後の展望:季節変化に寄り添う時計の意義】
自然界の環境リズムは、常に変化しています。夏は日が長く、冬は日が短くなります。季節や環境の変化という厳しい試練の中で命を繋ぐために、体内時計がどのような役割を担っているかを今後の研究で明らかにしたいと考えています。
植物発生研究室:水田百香「ゼニゴケ仮根における伸長方向の制御機構の解析」
【研究の背景】細胞は自らの持つ極性や環境刺激を手掛かりにし、方向を認識して成長することで多様な形態を作ります。植物における成長方向の制御因子として、NIMA関連キナーゼ(NEK)が挙げられます。NEKはゼニゴケにおいて、仮根の伸長方向を制御しています。ゼニゴケは、陸上植物の進化において初期に分岐した植物で、扁平な器官である葉状体が分岐しながら成長し、その地面側の表皮から、単細胞性の仮根が重力方向に伸長します(図1)。仮根は土壌への固着と水分・養分の吸収を行う原始的な根系です。ゼニゴケNEKは、仮根先端に形成される微小管束に集積し、微小管をリン酸化して過剰な微小管を除去することで成長方向を安定化させると考えられています(図1)。最近、NEKは微小管付随タンパク質やその他の多数のタンパク質と相互作用して機能することが示唆されました。しかし、仮根の伸長方向がどのように制御されているのか、その全貌は明らかになっていません。初期の根系と考えられる仮根をモデル系として解析することで、植物の成長制御とその進化が明らかになることが期待されます。
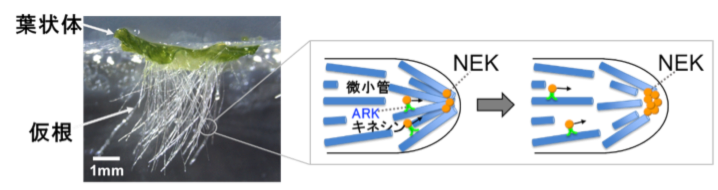
図1. ゼニゴケの形態と仮根伸長のしくみ
【研究内容】 ゼニゴケの成長機構を理解するために、NEKと相互作用するタンパク質の機能を解析しました。その結果、NEKと相互作用する因子には、微小管を制御するものと、仮根先端で顆粒状の構造を形成するものがあり、これらは微小管依存的に仮根先端に集積していることが明らかになりました。これらのタンパク質が複合体を形成し、ARKキネシンと呼ばれるモータータンパク質によって仮根先端へ輸送され、微小管束の動態や顆粒形成を制御することで伸長方向を決定している可能性が考えられます。また、NEK相互作用因子は仮根だけでなく葉状体の成長にも関与していることが明らかになりました。
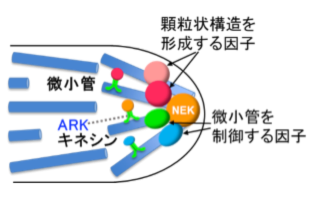
図2. 仮根細胞における複合体のモデル
【今後の研究予定】
これまでに得られた結果から、タンパク質をリン酸化して制御するキナーゼ(NEK)や仮根先端にタンパクやオルガネラを輸送するキネシンモーター(ARK)が中心となり、仮根先端にタンパク質複合体を形成し、成長方向を制御していると考えられます。博士後期課程では、様々なNEK相互作用タンパクの機能について解析を進め、仮根と葉状体の伸長方向がどのように制御されているのかを理解したいと考えています。
構造生命科学研究室:石井瑞樹「光合成で水を分解する仕組みの解明 −酸素発生複合体の中間状態構造の解析−」
【研究の背景】地球上の酸素の大部分は、植物や藍藻が行う光合成によって生み出されています。光合成では、太陽光のエネルギーを利用して水を分解し、酸素・電子・プロトンを生成します。この反応は、私たちが呼吸する酸素を供給するだけでなく、生態系全体のエネルギー循環を支える極めて重要な過程です。
この水分解反応を担っているのが、光化学系IIと呼ばれるタンパク質複合体です (図1)。その内部には「酸素発生複合体」と呼ばれる金属クラスターが存在し、ここで水分子が段階的に分解されます (図2)。この反応は、複数の中間状態を経ながら進行すると考えられており、それぞれの状態で構造や電子の状態がどのように変化するかを理解することが、反応機構の解明に直結します。
しかしながら、これらの中間状態の詳細な構造は十分に明らかになっていません。特に、特定の条件で現れる「高スピン状態」と呼ばれる電子状態は、次の反応段階へ進む鍵となる可能性が指摘されていますが、その実体は理論的なモデルにとどまっており、実験的な検証が求められています。こうした背景から、光合成における水分解の仕組みを原子レベルで理解することが、基礎科学のみならず、将来のエネルギー技術にもつながる重要な課題となっています。
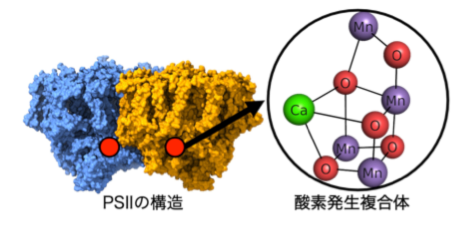
図1 PSIIと酸素発生複合体の構造
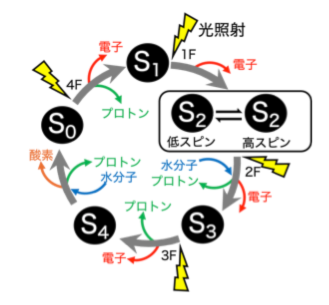
図2 光照射によるS状態の遷移
【研究内容】 本研究では、藍藻由来の光化学系IIを対象に、特に水分解反応の途中段階であるS2状態に着目しています。アルカリ性条件では高スピン状態が増加することが知られており、この条件を利用して構造解析を行っています。
具体的には、X線自由電子レーザーを用いたアルカリ性条件下での結晶構造を解析し、pHや酸素発生複合体の酸化状態が異なる条件下での構造の違いを比較することで、反応中間体の特徴を明らかにしようとしています。また、酸素発生複合体そのものだけでなく、その周囲に存在するプロトンや電子の移動に関わる領域にも注目し、反応全体の流れを構造的に理解することを目指しています。この研究のこれまでの成果をまとめて、2026年にリバプールで開催される国際光合成学会の会議にてポスター発表をする予定です。
【今後の研究(展望)】
今後は、より高精度な構造解析や理論計算との比較を通じて、水分解反応の各段階における詳細な変化を明らかにしていきたいと考えています。特に、高スピン状態の正確な構造や、プロトンおよび電子の移動機構を理解することが重要な課題です。
これらの知見は、光合成の基本原理の理解を深めるだけでなく、太陽光を利用した人工的なエネルギー変換技術の開発にも貢献することが期待されます。
構造生命科学研究室:米田耕士 「イネ由来アルミニウム輸送体の構造解析」
【研究の背景】アルミニウムは土壌中に3番目に多く存在する元素で、pH 5.5以下の酸性条件で溶け出し、作物の生育を著しく阻害するアルミニウム毒性を引き起こします。地球上の耕作地のうち約30%はアルミニウム毒性の影響が大きい酸性土壌です。そのためアルミニウム毒性は世界の穀物の収量低下の主要要因となっており、また酸性土壌の改良に伴う生産コストの増大につながることから、食料の安定供給の課題となっています。
イネ(Oryza sativa)は高いアルミニウム耐性を持つ植物として知られており、そのアルミニウム耐性機構を詳細に理解することは、アルミニウム耐性の高い作物を作出するために重要です。イネのアルミニウム耐性では複数の輸送体を発現し、葉や茎など影響の少ない器官に輸送し、隔離する方法がとられています。私の研究では液胞隔離に関与する輸送体の研究を行っています。しかし、アルミニウム輸送体がどのようにアルミニウムを輸送しているのか、その詳細は不明です。私は、アルミニウム輸送機構の解明を目指し、アルミニウム輸送体の構造研究に取り組んでいます。
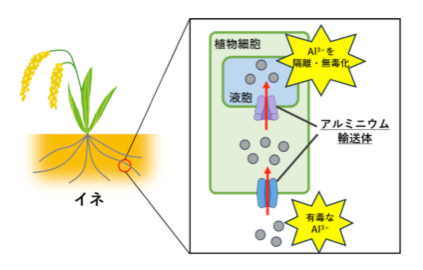
図1 アルミニウムが液胞へと隔離される様子
【卒論・修論の内容】 アルミニウム輸送機構を明らかにするために岡山大学のクライオ電子顕微鏡を用いて単粒子構造解析を行いました(図2)。その結果、これまでに基質が結合する直前の内向き構造と輸送サイクルが始まる前の閉塞構造を得ました。タンパク質内部には親水性のアミノ酸残基で構成されるポケットがありアルミニウム結合部位と想定されました。

図2 構造解析の流れ
【今後の予定】
得られた構造情報を基に、アルミニウム結合に関与するアミノ酸残基の変異体を作製し、それらの輸送活性を測定し、変異の影響を評価します。最終的に構造解析と機能解析の結果を統合し、輸送に重要な構造変化やアミノ酸残基を特定し、アルミニウム輸送機構を明らかにしたいと考えています。







