腫瘍融解ウイルス「テロメライシン」のがん幹細胞に対する抗腫瘍効果を証明
2013年12月18日
岡山大学大学院医歯薬学総合研究科消化器外科学分野の藤原俊義教授、矢野修也医師、カリフォルニア大学サンディエゴ校(外科)のRobert Hoffman教授らの研究グループは、オンコリスバイオファーマ株式会社(本社:東京都港区、代表取締役社長:浦田泰生)が臨床開発を進める腫瘍融解ウイルス「テロメライシン」が、休眠状態にある細胞周期を回転させることで、効率よく胃がん幹細胞を殺傷することを世界で初めて明らかにしました。
本研究成果は2013年12月1日、米国科学雑誌『Clinical Cancer Research』に掲載され、同号の「Highlights」にも選出されました。
がんの根源を成すがん幹細胞は、抗癌剤や放射線に抵抗性を示し、がんの再発につながっていると考えられています。今後、「テロメライシン」の治療により、がん幹細胞を含めたがんの根治が期待されます。
<業 績>本研究成果は2013年12月1日、米国科学雑誌『Clinical Cancer Research』に掲載され、同号の「Highlights」にも選出されました。
がんの根源を成すがん幹細胞は、抗癌剤や放射線に抵抗性を示し、がんの再発につながっていると考えられています。今後、「テロメライシン」の治療により、がん幹細胞を含めたがんの根治が期待されます。
がんの根源を成す「がん幹細胞」は、分裂して自分と同じ細胞を作り出すことができる「自己複製能」とともに、いろいろな細胞に分化することのできる「多分化能」を有しています。つまり、がん幹細胞を根絶しなければ、がんの根治は難しいと考えられています。
がん幹細胞は、分裂停止状態に留まることができ、多くの場合、細胞周期が静止した「休眠状態」にあります。そのため、増殖期にある細胞に有効な抗がん剤や放射線に抵抗性を示し、がんの再発の原因となります。
今回、藤原教授らの研究グループは、細胞周期のG1期にある細胞を「赤色」、S期にある細胞を「黄色」、G2/M期にある細胞を「緑色」の蛍光でみることができる胃がん細胞を樹立し、がん幹細胞のマーカーであるCD133陽性の細胞をフローサイトメトリーで分離してきました。その分離したCD133陽性の胃がん幹細胞をスフェロイド培養(三次元培養)したところ、すべての細胞は赤色でG1期に止まっており、抗がん剤(シスプラチン)や放射線でも癌細胞塊の大きさは変わりませんでした。
一方、腫瘍融解ウイルスである「テロメライシン®」の投与により、癌細胞塊の表面から細胞は黄色や緑に変わり、徐々に癌細胞塊のサイズが減少して、最終的には胃がん幹細胞のスフェロイドは消滅しました(図1)。
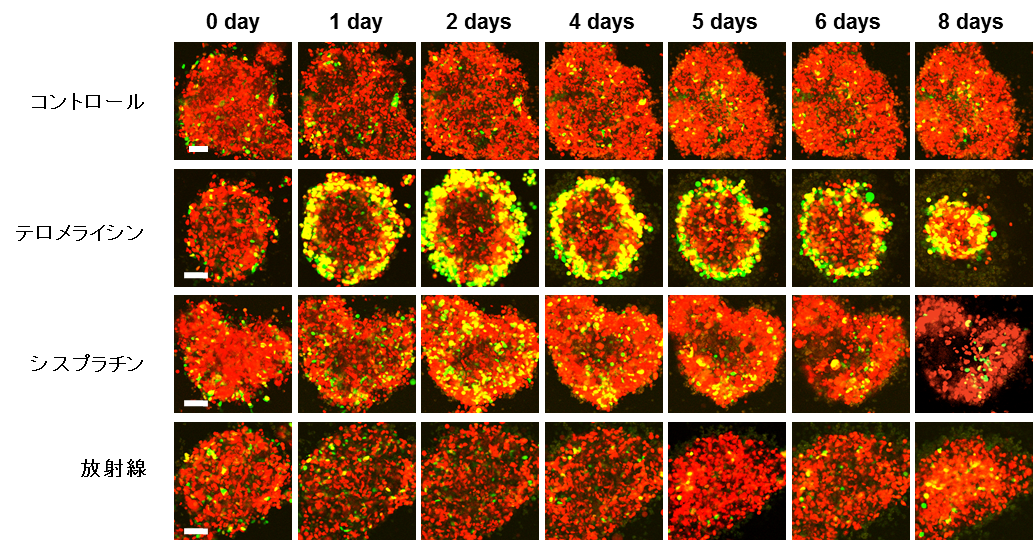
図1.テロメライシンによる休眠癌幹細胞の活性化と細胞破壊
ウイルスは本来、自らのDNAを複製するために感染した細胞の細胞周期を回転させる機能があり、「テロメライシン」は胃がん幹細胞の細胞周期を止めているp53やp21の発現を抑え、逆に細胞周期を回転させるE2F-1の発現を上げることが本研究結果から示されました。さらに、マウス移植した腫瘍の中心部のがん細胞も休眠状態にありましたが、「テロメライシン」の投与で細胞周期が回転して効率よく細胞死が誘導されることが明らかとなりました。
<見込まれる成果>
がんは1981年以来、日本人の死亡原因の第1位を占めており、国民の健康と安全・安心な社会を確保するためには、既存の治療コンセプトとは異なる革新的な治療技術の開発が不可欠です。「テロメライシン」は、テロメラーゼ活性を標的とするがん治療を目的とした生物製剤で、生体内で自立性を持って増殖することによって従来の抗がん剤にない抗腫瘍効果の作用機序を有しています。
今回の研究成果は、細胞周期を検討することで「テロメライシン」が理論的にがん幹細胞に有効であることを示しており、がんの再発を防ぎ、根治を目指した治療戦略の確立に有用であると考えられます。今後、「テロメライシン」の臨床開発が順調に進むと、がん幹細胞にも有効な革新的な抗がんウイルス製剤として、国民の健康増進や医療経済の節減にも役立つと期待されます。
<補 足>
テロメライシンとは:
「テロメライシン」は、風邪ウイルスの一種であるアデノウイルスのE1領域に、多くのがん細胞で活性が上昇しているテロメラーゼという酵素のプロモーターを遺伝子改変によって組込み、がん細胞中で特異的に増殖して、癌細胞を破壊することができるようにしたウイルス製剤です。
「テロメライシン」がヒトのがん細胞に感染すると、一日で10万~100万倍に増え、がん細胞を破壊します。
一方、「テロメライシン」は正常組織細胞にも同様に感染はしますが、テロメラーゼ活性がないためウイルスは増殖せず、正常組織での損傷は少ないと考えられます。
オンコリスバイオファーマ株式会社が米国で実施した、がん患者に対する「テロメライシン」の臨床試験において、重篤な副作用は認められておらず、一部の患者では投与部位での腫瘍縮小効果などの有効性が認められています。
発表論文はこちらからご確認いただけます
発表論文:Yano S, Tazawa H, Hashimoto Y, Shirakawa Y, Kuroda S, Nishizaki M, Kishimoto H, Uno F, Nagasaka T, Urata Y, Kagawa S, Hoffman RM, Fujiwara T. A genetically engineered oncolytic adenovirus decoys and lethally traps quiescent cancer stem-like cells into S/G2/M-phases. Clin Cancer Res. December 1, 2013 19:6495-6505.
報道発表資料はこちらをご覧ください
<お問い合わせ>
(所属)岡山大学大学院医歯薬学総合研究科 消化器外科学分野 教授
(氏名)藤原 俊義
(電話番号)086-235-7257
(FAX番号)086-221-8775
(URL)http://www.ges-okayama-u.com/