シャペロンによるビタミンB12酵素再活性化の分子機構を解明
2014年01月27日
岡山大学の虎谷哲夫名誉教授と同大大学院自然科学研究科の森光一助教らの研究グループは、ビタミンB12関与酵素の再活性化シャペロンである「ジオールデヒドラターゼ再活性化酵素(DD-R)」のヌクレオチドスイッチとサブユニットスワッピングに関与するアミノ酸残基を同定しました。
本研究成果は、虎谷名誉教授らが世界に先駆けて発見した3種のビタミンB12酵素再活性化シャペロンの中で最も研究が進んでいるDD-Rを用いて、不活性化されたビタミンB12酵素の再活性化の分子機構を解明したものです。2013年12月3日、アメリカの生物化学系国際雑誌『Biochemistry』に掲載されました。
ビタミンB12酵素の再活性化シャペロンを応用すれば、原理的にはビタミンB12酵素の不活性化の問題が解決できます。それにより、1例を挙げれば、植物油からバイオディーゼル燃料を製造した後の廃液から夢の合成繊維材料ポリトリメチレンテレフタレート*1の原料であるトリメチレングリコールを製造したり、廃油をエネルギー源と炭素源として完全再資源化することも可能になると期待されます。
<業 績>本研究成果は、虎谷名誉教授らが世界に先駆けて発見した3種のビタミンB12酵素再活性化シャペロンの中で最も研究が進んでいるDD-Rを用いて、不活性化されたビタミンB12酵素の再活性化の分子機構を解明したものです。2013年12月3日、アメリカの生物化学系国際雑誌『Biochemistry』に掲載されました。
ビタミンB12酵素の再活性化シャペロンを応用すれば、原理的にはビタミンB12酵素の不活性化の問題が解決できます。それにより、1例を挙げれば、植物油からバイオディーゼル燃料を製造した後の廃液から夢の合成繊維材料ポリトリメチレンテレフタレート*1の原料であるトリメチレングリコールを製造したり、廃油をエネルギー源と炭素源として完全再資源化することも可能になると期待されます。
岡山大学の虎谷哲夫名誉教授と同大大学院自然科学研究科の森光一助教らの研究グループは、ビタミンB12関与酵素の再活性化シャペロンである「ジオールデヒドラターゼ(DD)再活性化酵素(DD-R)」のヌクレオチドスイッチとサブユニットスワッピング*2に関与するアミノ酸残基を同定しました。
虎谷名誉教授らは、ビタミンB12が補酵素として関与する酵素を再活性化する分子シャペロン*3 3種類を世界に先駆けて発見し、それらの構造と作用機構の研究を先導してきました。本研究はその中で最も研究が進んでいるDD-Rを用いて、不活性化されたB12酵素の再活性化の分子機構を明らかにしたものです。
ビタミンB12はコバルトを含む錯体で、生体内で補酵素型(ビタミンB12補酵素、図1A)に変換され、酵素の活性部位に結合してその触媒作用を助けます。ビタミンB12補酵素はコバルト−炭素(Co-C)結合を含む複雑な構造と重要な生理機能により、理、工、農、薬、医など多くの分野の研究者らを魅了してきました。ビタミンB12補酵素が関与する酵素(以下、B12酵素)は、化学的に起こり難い反応を触媒するため、ラジカル*4という超活性種を活用しています(図1B)。ラジカルは、反応性が高い反面、副反応を起こして消滅し易く、その結果補酵素が損傷を受けます。損傷補酵素が酵素から離れないため、B12酵素は不活性化され易いという宿命があります。
虎谷名誉教授らは、B12酵素の触媒機構を詳細に研究する過程で、不活性化されたB12酵素を再活性化するタンパク質3種類を世界に先駆けて発見し、「再活性化因子」または「再活性化酵素」と名付けました(図1B)。
これらのタンパク質はシャペロン*3の1種で、ヌクレオチド依存的にB12酵素と固く結合し、損傷補酵素を解離させることで、B12酵素を再活性化するという作用機構を解明しました。さらに再活性化シャペロンの立体構造を解析し(図1C)、類似した構造のサブユニットをもつ酵素との間でサブユニットスワッピングにより複合体が生成すること、およびこの複合体中で誘起される立体反発により損傷補酵素が解離するという機構を明らかにしました。しかし、ヌクレオチド依存的に酵素との結合性が変化し、シャペロン機能が発現するという「ヌクレオチドスイッチ」とサブユニットスワッピングに関与するアミノ酸残基については不明のままでした。
虎谷名誉教授と森助教らは、3種類のB12酵素再活性化シャペロンと熱ショックタンパク質Hsp70が全体的には似ていないものの、アミノ酸配列が局所的に類似した領域が3カ所存在し、それらがADP結合部位の3つのループに対応することをDD-RのX線構造解析により解明していました(図1D)。
今回、これらの局所的類似領域のアミノ酸残基に変異を導入して調べた結果、いずれのループもDD-Rの機能に必須であることが分かり、ATPの加水分解に重要なAsp残基とATP-ADPスイッチに重要なAsp残基とを同定することにも世界ではじめて成功しました(図1F)。また、DD-Rのサブユニット界面に存在するMg2+の役割に着目し(図1E)、Mg2+に配位している残基に変異を挿入するとDD-R機能が失われることを示しました。
さらに、このMg2+に配位するGlu残基を含む(Glu)3クラスター領域がB12酵素DD側にも存在することに注目し(図1C)、真ん中のGluをGln残基で置換すると、DDがDD-Rによる再活性化を受けられなくなることも分かりました。これらの研究成果により、DD-Rのヌクレオチドスイッチ機構の一端が解明され、また、Mg2+への配位がサブユニットスワッピングとDDの再活性化に不可欠であることが明らかとなりました。
今後、非加水分解性ATPアナログが結合したDD-Rの立体構造を解明することで、B12酵素再活性化シャペロンのヌクレオチドスイッチの精密な機構が解明されると期待されます。
<脚 注> *1 優れた物性をもつ合成繊維材料ポリトリメチレンテレフタレートのこと。*2 2つのタンパク質の間でサブユニットの交換が起こること。*3 「若い貴婦人が社交界にデビューするときの介添え役」というのがもともとの意味であるが、転じて分子の世界で「タンパク質が正しく折り畳まれて立体構造を形成するのを助けるタンパク質」を分子シャペロンまたは単にシャペロンと呼ぶ。*4 不対電子をもつ化学種のこと。一般に反応性がきわめて高い。
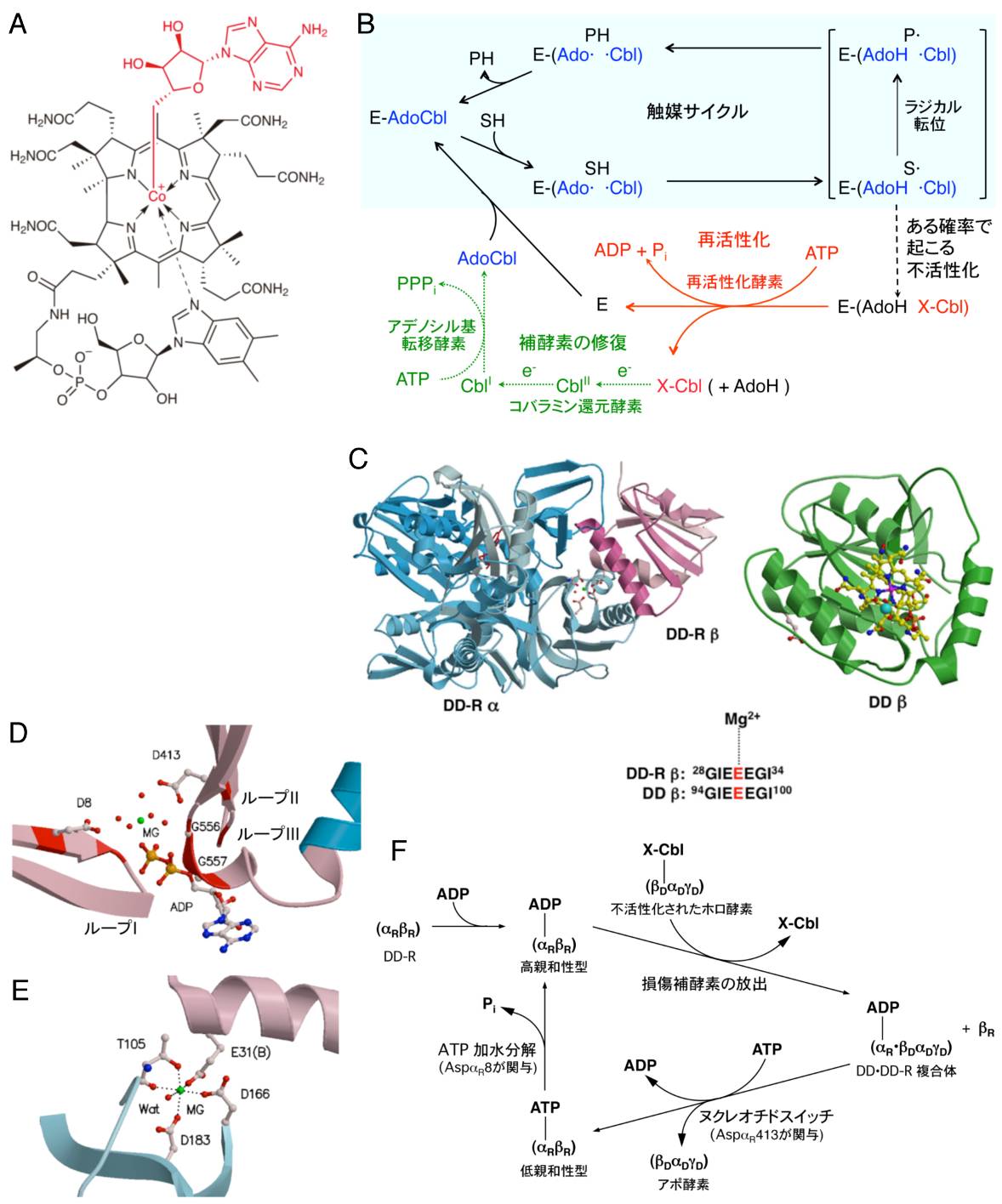
(A) B12補酵素(アデノシルコバラミン; AdoCbl)(B) 触媒機構と補酵素リサイクリングの概略。AdoCblが関与する酵素はラジカル機構で触媒する(基質はSH、生成物はPH)。ラジカル中間体のいずれかが副反応を起こしてラジカルが消滅すると、補酵素が再生されず、生じた損傷補酵素(X-Cbl)が酵素から離れないため酵素は不活性化される。再活性化酵素として働くシャペロンはATP存在下で、強固に結合しているX-Cblを酵素から解離させる。生じたアポ酵素(E)はAdoCblと結合して活性なホロ酵素を再構成する。X-Cblはコバラミン還元酵素とアデノシル基転移酵素によりAdoCblに再生される。(C) DD-Rと酵素DDのサブユニットの構造類似性(D) DD-RのADP結合部位(E) DD-RのMg2+結合部位(F) 不活性化されたホロ酵素の再活性化機構
(パネルC〜Fの図は今回の発表論文から引用)
発表論文はこちらからご確認いただけます
発表論文:Mori K, Obayashi K, Hosokawa Y, Yamamoto A, Yano M, Yoshinaga T, and Toraya T. Essential roles of nucleotide-switch and metal-coordinating residues for chaperone function of diol dehydratase-reactivase. Biochemistry, 52, 8677-8686 (2013). dx.doi.org/10.1021/bi401290j.
報道発表資料はこちらをご覧ください
<お問い合わせ>
岡山大学名誉教授
虎谷 哲夫
(メールアドレス)pekotora2007(at)yahoo.co.jp
※ (at)を@に置きかえてください。