酵素[NiFeSe]ヒドロゲナーゼの分子進化メカニズムを解明-酵素の分子進化を立体構造で理解する新たな解析手法-
2016年01月28日
国立大学法人 岡山大学
国立研究開発法人 科学技術振興機構
国立研究開発法人 科学技術振興機構
本研究のポイント・ 酵素の分子進化は系統樹解析に基づいて、アミノ酸配列の比較のみが議論されてきたが、立体構造情報に基づいて酵素機能を議論する方法がなかった。・ 配列情報から信頼性の高い立体構造情報を計算する手法を確立し、酵素の分子進化を立体構造の変遷として再現することに世界で初めて成功した。・ バクテリア種の系統樹解析に基づく宿主の環境適応モデルと、今回開発した立体構造計算化学の組み合わせによる手法が普及することにより、タンパク質の分子進化研究が大きく前進することが期待される。
岡山大学大学院環境生命科学研究科(農)農生命科学専攻の田村 隆教授の研究グループは、系統樹解析から得られたアミノ酸配列情報に基づき、スーパーコンピューターを用いて信頼性の高い立体構造を再現する斬新な計算化学の手法を確立しました。この手法を用いて、硫酸還元菌の水素代謝酵素の一つである[NiFeSe]ヒドロゲナーゼの立体構造を再現することで、微生物が、生息する環境の酸素曝露リスクに応じて、酵素の立体構造を大胆に変化させてきた経緯と精緻なメカニズムを解明しました。本研究成果は1月28日(英国時間午前10時)、英国の科学雑誌「Scientific Reports」に掲載されます。
現在、地球上の生物が持つさまざまなタンパク質は、共通祖先から派生して分化してきたと理解され、その系統関係が議論されています。しかし、これまで進化の数理モデルで復元されてきたのはアミノ酸配列までで、タンパク質の機能解明に必要な立体構造として考察することはできませんでした。本研究グループは、配列情報からタンパク質の立体構造に踏み込み、微生物の環境適応を酵素の分子進化の観点から考察し、立体構造の変遷を再現する新たな解析方法を見いだしました。
本研究成果は、酵素の分子進化を立体構造の変遷として考察する新しい概念を提供しただけでなく、本解析を用いた最適酵素の選択などによる熱損失のないバイオ燃料電池の開発や、地球規模の環境の変化を知る新たな手がかりにつながると期待されます。
本研究は、科学技術振興機構(JST)の戦略的創造研究推進事業 個人型研究(さきがけ)の一環として行われたものです。現在、地球上の生物が持つさまざまなタンパク質は、共通祖先から派生して分化してきたと理解され、その系統関係が議論されています。しかし、これまで進化の数理モデルで復元されてきたのはアミノ酸配列までで、タンパク質の機能解明に必要な立体構造として考察することはできませんでした。本研究グループは、配列情報からタンパク質の立体構造に踏み込み、微生物の環境適応を酵素の分子進化の観点から考察し、立体構造の変遷を再現する新たな解析方法を見いだしました。
本研究成果は、酵素の分子進化を立体構造の変遷として考察する新しい概念を提供しただけでなく、本解析を用いた最適酵素の選択などによる熱損失のないバイオ燃料電池の開発や、地球規模の環境の変化を知る新たな手がかりにつながると期待されます。
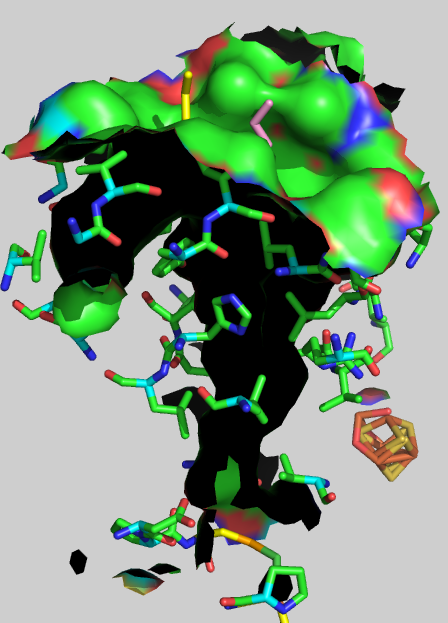
ある種の[NiFeSe]ヒドロゲナーゼは水素を取り込むために大きく開口したガス・キャビティを持つ (キャビティ形成に関わるアミノ酸残基をスティック構造で表記し、キャビティ壁面を黒色で表記した) 。
田村教授らの研究グループは、公開されている硫酸還元菌のゲノム情報から新たに9種の[NiFeSe]ヒドロゲナーゼを発見し、セレン含有ヒドロゲナーゼのファミリーが普遍的な[NiFe]型から派生した共通祖先に由来する系統であることを突き止めました。また、セレノシステイン(Sec)残基を翻訳するための特殊な翻訳装置を構成する遺伝子群が[NiFeSe]ヒドロゲナーゼの分子進化に伴って継承されてきたことも発見しました。細菌では種の系統をたどることは極めて困難とされてきましたが、複数のマーカー遺伝子群の発見により細菌の種の系統をたどる道筋を示すことができました。同時に硫酸還元菌の共通祖先菌が地球上のさまざまな生息環境に適応しながら種の多様性を拡大させてきた背景に[NiFeSe]ヒドロゲナーゼの分子進化が深く関わってきたことも示されました。
次に本研究グループは、密度汎関数を用いた力場パラメータやタンパク質の分子内相互作用の最適化計算などを分子動力学計算に取り込み、スーパーコンピューターを駆使して配列情報から信頼性の高い構造情報を計算する斬新な計算化学の手法を確立しました。この手法を用いて、今回発見した9種類を含む全ての[NiFeSe]ヒドロゲナーゼのアミノ酸配列を立体構造として再現しました。その結果、ある種の[NiFeSe]ヒドロゲナーゼが持つ巨大な穴(ガス・キャビティ)は、深海の熱水噴出口のような酸素が存在せずに水素が潤沢に供給される環境に適応した菌において形成されたものであり、日中は陽光が差し込み酸素を発生する光合成生物が繁殖する浅瀬の堆積層に生息する菌では、ガス・キャビティが閉じた立体構造を維持してきたことがわかりました。ガス・キャビティの構造の差は、微生物が生息する環境の酸素曝露リスクに応じて、立体構造を大胆に変化させてきた経緯とメカニズムを示しています。
本研究成果は、系統樹として算出された配列情報を生物学的に意味のある立体構造として描くことができた最初の研究成果であり、酵素の分子進化を立体構造の変遷として考察できることを提案した画期的成果でもあります。従来、不可能とされてきたことを可能にした革新的な本研究成果は、タンパク質の分子進化研究に大きく寄与すると共に、将来的な産業応用にも大きな波及効果をもたらすことが期待されます。
<背 景>
ヒドロゲナーゼ
水素代謝酵素ヒドロゲナーゼには、[FeFe]型、[NiFe]型、セレンを含有する[NiFeSe]型がありますが、このうち[NiFeSe]ヒドロゲナーゼは2%程度の酸素存在下でも水素製造能力を維持する高い酸素耐性を持つことで世界的に注目されています。[NiFeSe]ヒドロゲナーゼは、これまでに3種の硫酸還元菌の中でのみ存在が知られていました。
今回、本研究グループは、高い酸素耐性を持つ[NiFeSe]ヒドロゲナーゼを、さまざまな生息環境に分布する9種の細菌から新たに発見しました。これらの新規な[NiFeSe]ヒドロゲナーゼの分子系統の解明に取り組みました。
タンパク質の分子進化の解析
酵素などのタンパク質の分子進化は、系統樹解析に基づいてアミノ酸配列の比較のみが議論されています。しかし、アミノ酸配列の比較では、立体構造の変遷が描けないため、何が淘汰されて何が継承されたのか、進化と適応の具体的かつ本質的な経緯が議論されていません。これまで、タンパク質の機能を理解する上で立体構造が必須であることは広く認識されていましたが、配列情報から信頼性の高い構造情報を計算する手法が確立されていなかったため、立体構造の変遷を考察できませんでした。
<見込まれる成果>
構造計算化学を取り入れた酵素の分子進化研究
本研究成果によって、タンパク質の分子進化を配列の比較だけでなく、立体構造の変遷に基づいて考察できることが示されました。分子進化を経て、微妙に変わっていくアミノ酸配列の裏で、タンパク質の立体構造に何が起きているのか、タンパク質の構造の変遷を計算化学の手法で再現する解析法は広く活用されることが期待されます。
バイオ燃料電池
本研究の解析によって提示された12種類の[NiFeSe]ヒドロゲナーゼは、キャビティのサイズと形状に基づいて、高い酸素耐性が期待できる閉塞型酵素と、高い水素吸収能を特長とする開口型酵素などのバリエーションがあります。
今後、本解析法を用いて燃料電池の用途と目的に応じて最適な酵素を選択することができれば、熱損失のない水素と電気を相互変換するバイオ燃料電池の開発が期待されます。
バクテリア種の系統解析
バクテリア(細菌)では、遺伝子がある種から別の種に高い頻度で移動することがあるために、個々の遺伝子の系統関係に基づいて種の系統関係を考察することが困難でした。
本研究成果から、セレン含有酵素の生合成に関わる複数の遺伝子がゲノム上に散在しており、これらをマーカー遺伝子群として系統関係を比較することで、バクテリア種の系統関係を明確に解析できました。本解析法によりバクテリアの系統関係が明らかになったので、その局在と分離源から地球規模の環境の変遷を解明できると期待されます。
本成果は、以下の事業・研究領域・研究課題によって得られました。
JST戦略的創造研究推進事業研 究 領 域 「藻類・水圏微生物の機能解明と制御によるバイオエネルギー創成のための基盤技術の創出」(研究総括:松永 是 東京農工大学 学長)研究課題名 好気条件下で水素(H2)製造反応を触媒する[NiFeSe]型ヒドロゲナーゼの分子構築研 究 者 岡山大学大学院環境生命科学研究科農生命科学専攻 教授 田村 隆研究実施場所 岡山大学大学院環境生命科学研究科研 究 期 間 平成23年10月~平成27年3月
JST戦略的創造研究推進事業研 究 領 域 「藻類・水圏微生物の機能解明と制御によるバイオエネルギー創成のための基盤技術の創出」(研究総括:松永 是 東京農工大学 学長)研究課題名 好気条件下で水素(H2)製造反応を触媒する[NiFeSe]型ヒドロゲナーゼの分子構築研 究 者 岡山大学大学院環境生命科学研究科農生命科学専攻 教授 田村 隆研究実施場所 岡山大学大学院環境生命科学研究科研 究 期 間 平成23年10月~平成27年3月
<論文情報>掲 載 誌 Scientific Reportsタ イ ト ル Molecular evolution of gas cavity in [NiFeSe] hydrogenases resurrected in silico著 者 Takashi Tamura, Naoki Tsunekawa, Michiko Nemoto, Kenji Inagaki, Toshiyuki Hirano, Fumitoshi SatoD O I 10.1038/srep19742
<お問い合わせ>
岡山大学大学院環境生命科学研究科(農)農生命科学専攻 教授 田村 隆
TEL:086-251-8293 FAX:086-251-8388
<JST事業に関すること>
科学技術振興機構 戦略研究推進部 川口 哲
TEL:03-3512-3525 FAX:03-3222-2064
<報道担当>
岡山大学 広報・情報戦略室
TEL:086-251-7292 FAX:086-251-7294
科学技術振興機構 広報課
TEL:03-5214-8404 FAX:03-5214-8432